GRIP大数据月报 | FDA 4月注册产品信息盘点及DeNovo产品信息概览

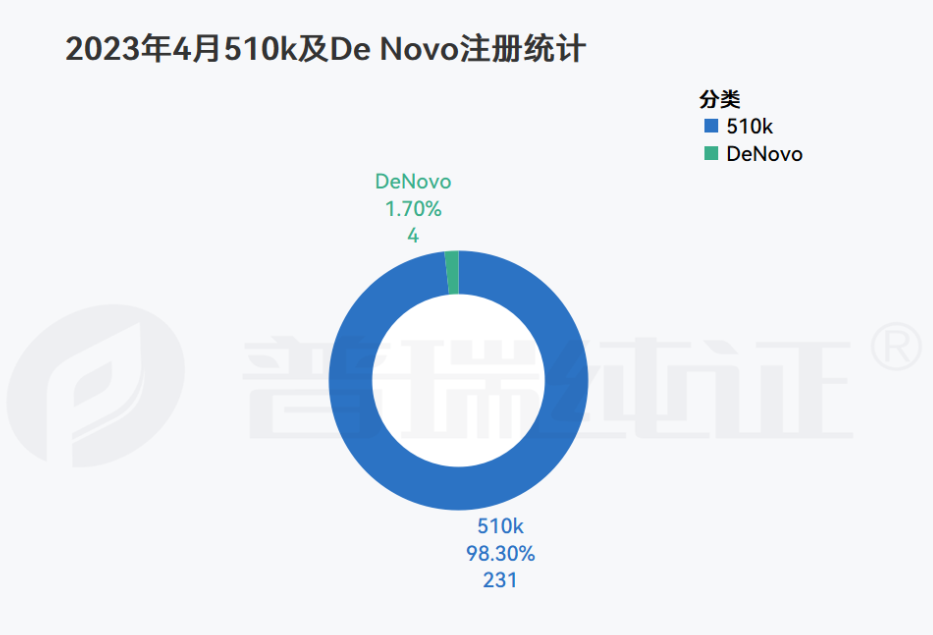
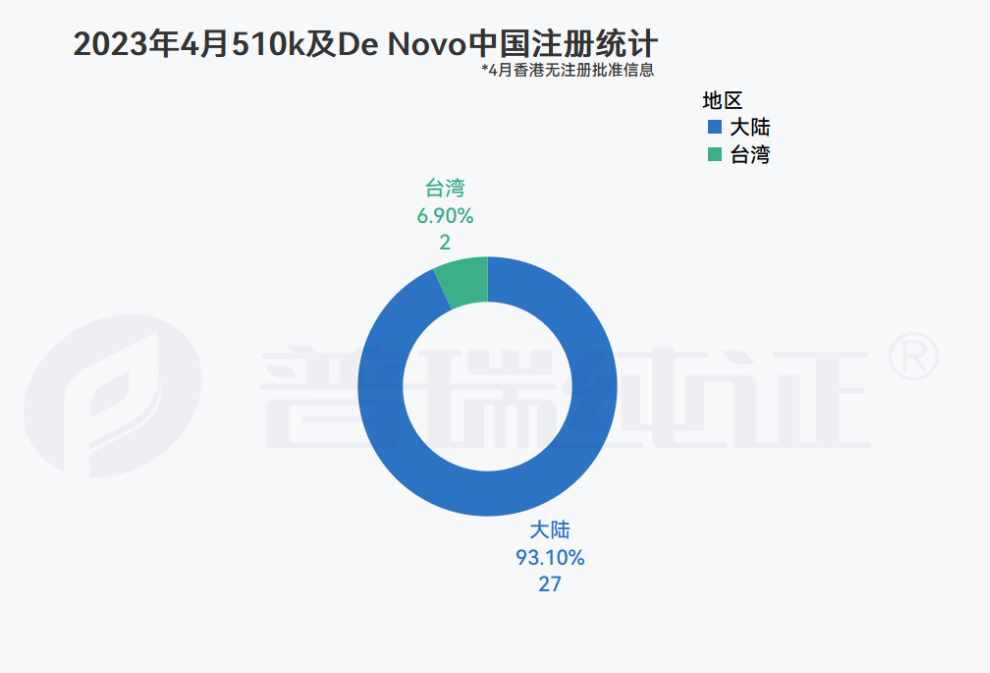
根据普瑞纯证GRIP大数据跟踪,FDA 于4月总计批准了235款医疗器械产品注册,231款510(K),4款DeNovo,其中中国厂商29款,全部集中在510(K)。
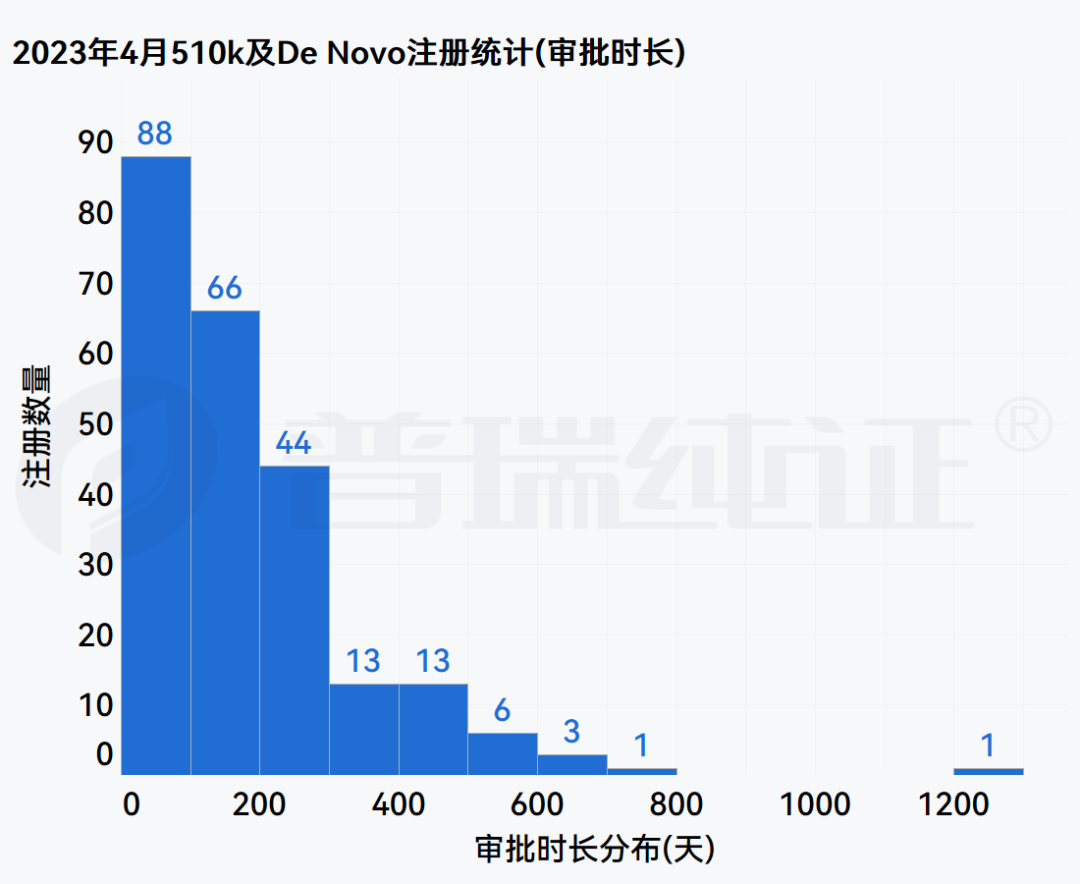
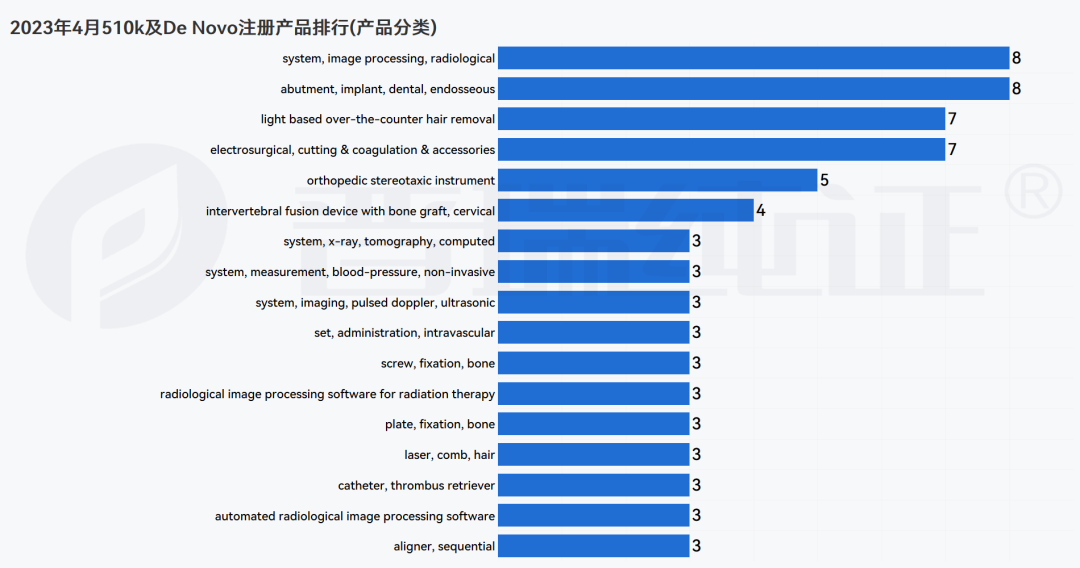
注册数量分布、注册时长分布及Product Code分布信息可查阅下方多图,更多法规、临床试验板块内容敬请关注后续更新的 《普瑞纯证&探针资本医疗器械行业月报4月版》内容。
左右滑动查看更多
在235款产品中,4款DeNovo产品的审批通过信息(按照时间先后),
由Candesant Biomedical, Inc. 申请的产品 The N-SWEAT Patch
由Moximed, Inc. 申请的产品 MISHA Knee System
由Noctrix Health, Inc. 申请的产品 NTX100 Tonic Motor Activation (NTX100 ToMAc) System
由Empower Medical Devices 申请的产品 Bateman Bottle
下面我们将依托GRIP数据对这四款产品进行一些信息的汇总。
The N-SWEAT Patch
由Candesant Biomedical, Inc. 申请的产品 The N-SWEAT Patch。

The N-SWEAT Patch商用名Brella,在2021年12月3日开始提交产品申报材料后,历时490天,完成产品的DeNovo注册,Product Code:QVX,该产品采用Candesant的专利:定向碱性热溶解(TAT)技术来减少过度的腋窝出汗,以及减轻日常活动中过度出汗带来的负面影响。
Candesant 的 TAT 技术利用钠与汗液中的水接触时产生热量的科学原理。将钠片敷在腋下时,产生的热能会精确定位到微目标汗腺,从而减少整体汗液的产生。据Candesant介绍,Brella是第一个利用钠与汗液反应的临床应用,也是唯一基于TAT技术的专利医疗器械。
FDA 对 Brella 的批准是基于SAHARA的临床试验数据,这是一项随机、双盲、假对照、多中心的关键研究,包括 110 名患有原发性腋窝多汗症的成年患者。患者的基线多汗症严重程度量表 (HDSS) 评分为 3 或 4,这表明过度出汗经常或总是干扰他们的日常生活。然后,患者在每个腋下接受最多 3 分钟的 Brella 或假贴剂双侧治疗。之后,在治疗后 12 周内每周对患者进行评估,对有反应的患者进行长达 24 周的随访。

SAHARA 研究的主要目标包括贴剂治疗后不良事件和皮肤反应的发生(2 周时间范围)以及 HDSS 评分达到 1 或 2(4 周时间范围)。关键的次要终点包括生活质量的平均改善以及治疗受试者的比例,从基线到 4 周,重力产汗量 (GSP) 至少改善 50%。符合条件的患者年龄在 22 岁或以上,每个腋窝的重力产汗量 (GSP) 大于 50mg。
从 2023 年夏末开始,Brella 将通过 Candesant Brella 早期体验计划在美国上市,该计划将包括具有美容实践和治疗多汗患者经验的医疗保健提供者。
MISHA Knee System
由 Moximed, Inc. 申请的产品 MISHA Knee System。
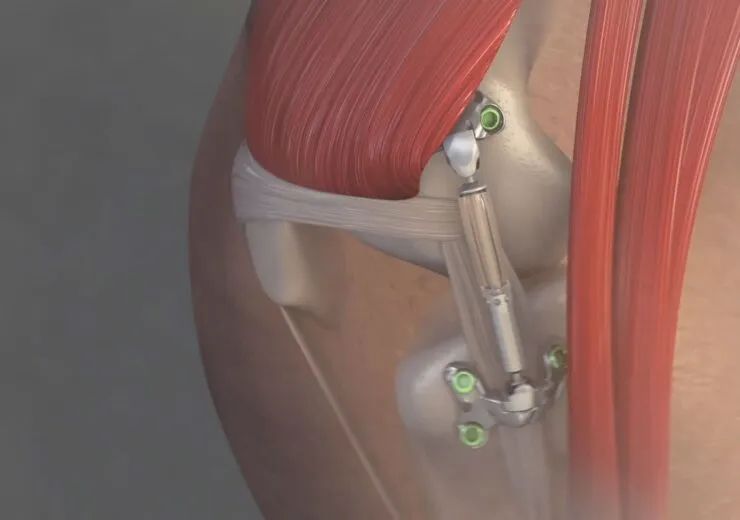
MISHA Knee System产品在2022年06月06日开始提交产品申报材料后,历时308天,完成产品的DeNovo注册,Product Code:QVV,MISHA是一种植入式减震器 (ISA),用于治疗膝关节内侧骨关节炎患者。
在最近的 Calypso 关键研究中发现,Moximed 能够证明MISHA优于高位胫骨截骨术 (HTO),这是一种成熟的手术。该公司利用减轻膝关节负荷的既定优势来设计该系统,该系统植入门诊兼容手术中。
FDA 官方表示此次授权的MISHA 膝关节系统,是一种放置在膝关节旁边的植入物,有助于减少部分关节承受的负荷量。与传统的膝关节置换不同,该设备不会移除膝关节。MISHA 膝关节系统适用于膝关节未能通过手术或非手术治疗后仍未能缓解疼痛的骨关节炎患者。

NTX100 Tonic Motor Activation System
由Noctrix Health, Inc. 申请的产品 NTX100 Tonic Motor Activation (NTX100 ToMAc) System。

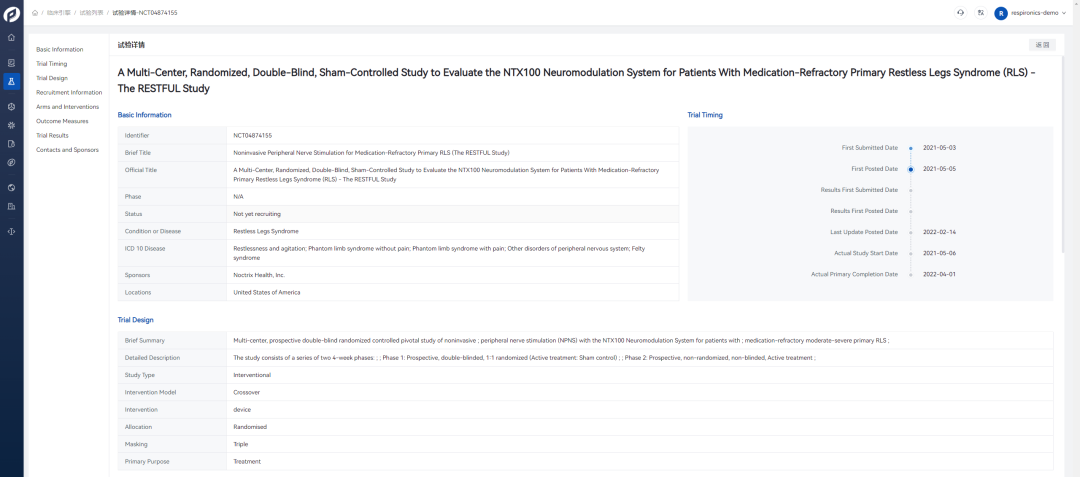
NTX100 Tonic Motor Activation (NTX100 ToMAc) System,在2022年9月21日开始提交产品申报材料后,历时208天,完成产品的DeNovo注册,Product Code:QWD,该产品旨在辅助改善药物难治性中度至重度不宁腿综合征 (RLS) 以改善患者睡眠质量。
NTX100 ToMAc 是一种仅限处方使用的设备,作为2020 年的突破性设备,产品通过通过减轻原发性中重度不宁腿综合征(RLS)的症状并改善耐药 RLS 患者的睡眠质量。
NTX100 ToMAc 是一种非侵入性系统,包括两个独立的治疗单元和两个放置在膝盖下方的独立电极贴片,可为腓神经提供高频、低水平的电刺激,腓神经为小腿提供运动和感觉、 脚和脚趾。患者可以通过治疗装置上的简单用户界面开始或停止刺激、调整强度等操作。除此之外,还配置了Clinician App 专供诊所和临床医生使用。临床医生可以使用医生端应用程序校准针对每位患者的治疗输出。
该产品同样储备了丰富的临床试验数据,通过共纳入133名药物治疗难治性RLS患者,以研究通过器械接入后的患者改良反应比例。
Bateman Bottle
由Empower Medical Devices 申请的产品 Bateman Bottle。在2022年11月21日开始提交产品申报材料后,历时150天,完成产品的DeNovo注册,Product Code:QVS,该产品是一种处方外科设备,利用真空吸力来帮助移除和容纳破裂的硅胶乳房植入物。
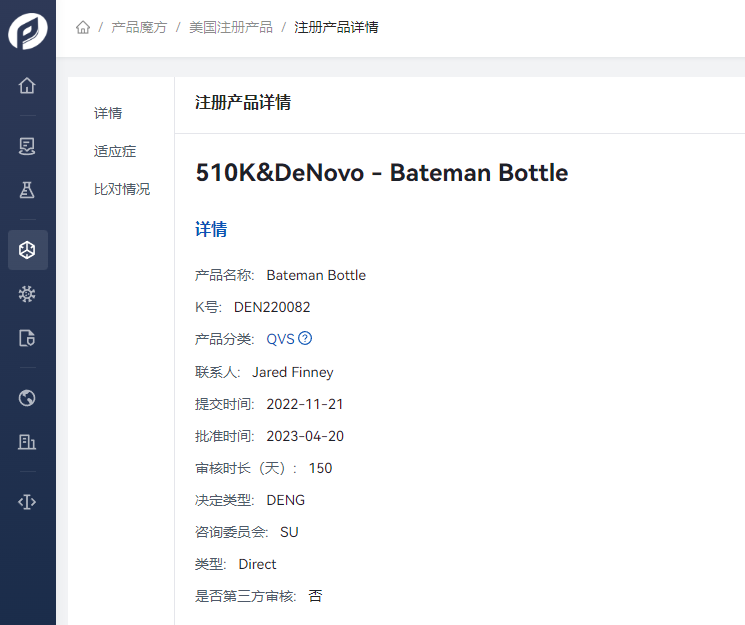
该产品作为乳房植入物移除系统(BIRS),这是一种一次性使用的吸力设备,用于帮助移除一个被胸膜囊包裹的破裂硅胶乳房植入物。

普瑞纯证作为中国医疗器械企业出海的好伙伴,致力于为客户提供全球的注册、临床试验的专业解决方案。如果您的产品在前往美国分销存在任何疑问,欢迎与我们的销售顾问进行沟通。如果你对我们的全球法规智能平台的数据感兴趣,也欢迎点击“阅读原文”进行注册体验或与您的销售顾问预约产品Demo时间。

-普瑞纯证官方咨询顾问-
-获取最新业内资讯-

关于我们
普瑞纯证是行业领先的全球化AI赋能生命科学服务商,我们的全球服务网络覆盖了包括中国、美国、英国、德国、荷兰、波兰、香港等多个国家和地区。
依托法规认证与临床经验丰富的全球顶尖专家服务团队,普瑞纯证为医疗器械、体外诊断产品等提供全球市场合规准入的全流程咨询服务,以及海外临床试验等一站式解决方案。100+ 国家准入,1000+ 海外注册/认证成功案例,60万+ 全球经销商数据,100万+ 全球临床试验数据,300万+ 全球医械注册数据。从市场战略到法规咨询,助力您的产品全方位顺利合规走向全球市场!