据360Dx报道,Siemens Healthineers的分子诊断业务正在寻找能够帮助其开发下一代高检测通量分子检测平台的合作伙伴,该平台计划在三年内在欧洲推出,意在与目前市场上的大容量分子检测系统竞争。
在西门子继续开发、销售现有的 Versant kPCR 分子诊断系统及配套检测试剂的同时,也在“在幕后努力寻找长期的最佳解决方案”,该公司的分子诊断负责人 Corey Bouwman,最近在葡萄牙里斯本举行的第 32 届欧洲临床微生物学和传染病大会 (ECCMID) 的期间说。 Versant kPCR分子诊断系统(提取设备+pcr仪)他说,公司期待其所有检测试剂,包括传统检测和开发中的检测,都将在新的分子诊断系统上运行。公司将把这个分子系统与 Atellica、其他临床化学和免疫测定测试系统一起销售,为其客户提供涉及所有模式的完整实验室解决方案。Bouwman在两年多前被任命为分子诊断负责人,他的目标是将公司的分子诊断产品整合到其实验室诊断产品组合中。该公司打算基于可运行 FTD开发的检测试剂的系统来定位目标医院和参考实验室客户。当然这个系统也要能运行西门子在收购FTD前后自己开发的项目。加上FTD,共有了 80 个适用于通用平台的分子检测项目,且都能够与 Versant kPCR 分子系统的传统测试菜单整合。
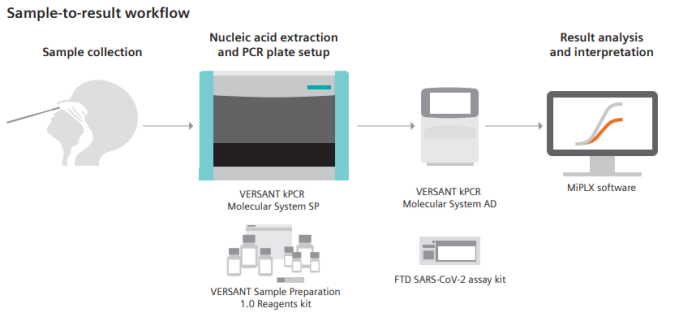
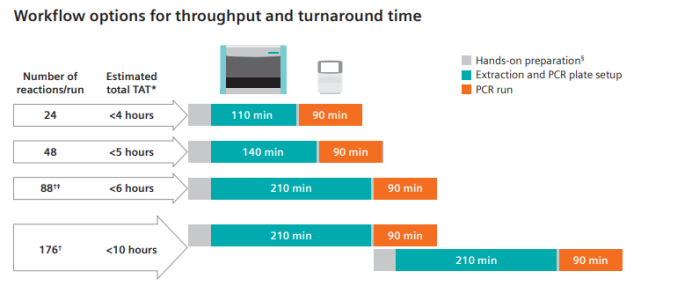
FDT是卢森堡的分子诊断测试开发商 Fast Track Diagnostics,西门子于2017 年 12 月收购据Bouwman所说,在 COVID-19 大流行爆发之前,Siemens分子诊断业务一直专注于 FTD 开发的测试菜单的业务,但随着疫情爆发,它迅速开发了基于Versant kPCR 分子系统的新冠分子检测。2020年4月,公司取得了SARS-CoV-2的检测和系统的CE。一个月后,美国食品和药物管理局批准了 SARS-CoV-2 测试的紧急使用,可基于梅里埃 EasyMag 提取系统和赛默飞7500 PCR仪使用。2020 年 7 月,FDA 授权更新该检测的使用说明,添加了Versant kPCR 分子系统为适用机型。Versant kPCR 分子系统产品资料:检测流程“虽然 Versant kPCR 一直是 SARS-CoV-2 和其他类型检测的一个很好的解决方案,但它也有局限性,现在客户想要的是最高水平的系统,让你能够随时随地加载您想要的任何检测,他们想要快速得到检测结果,而且不用任何人工操作,”Bouwman 说。Versant kPCR 分子系统产品资料:不同样本数所需时间示意图西门子 Versant kPCR 分子系统可在大约 5 个半小时内对96 个样品进行批量测试,预计总动手时间为 30 分钟。“考虑到可负担性及适用于批量检测的特点,此类批量测试的需求量仍然很大,但是最先进的检测系统的关键要素之一是完全自动化,”Bouwman 指出。这意味着在一个单一的工作流程中插入样本并获得结果,客户希望在两小时内完成测试,系统还得保持试剂又便宜仪器通量又高,他说。Siemens开发新的诊断测试平台的原因之一是,它预计到未来几年 PCR 测试需求将会增长。COVID-19 大流行改变了分子诊断测试的格局,提高了对该模式的认识。与此同时,随着实验室对 PCR 检测越来越熟悉,Siemens预计 PCR 检测需求将在广泛的条件下增加,以前从未进行过分子检测的实验室可能会有检测需求。
“我们知道市面上的很多分子诊断系统是专门为检测 SARS-CoV-2 而购买的,但其中大多数”无法运行足够广泛的测试菜单,因此也无法被视为 Siemens的下一个分子诊断平台的候选,他说。与其评估现在可以买到的可以用于分子检测的当前技术和系统 “我们坚信我们更应该拥有一个新平台,”他补充说,虽然分子试剂开发是 Siemens的核心能力,但分子测试系统开发能力不是。因此,该公司正在寻找合作伙伴——IVD 公司或学术合作者——可以与他们一起开发分子诊断测试平台,但根据 Bouwman 的说法,它正处于寻找的开始阶段。西门子医疗将致力于开发一个新平台,相比于罗氏、雅培和 Hologic 等公司已经在市场上的大通量分子诊断平台,新平台能提供更大的检测灵活性,相比于“昂贵”、低通量、基于卡盒的分子诊断测试,他能提供的检测价格更加可负担。(简单概括就是比COBAS8800一类的灵活,比分子POCT便宜)该公司预计三年内将新的分子诊断平台推向市场,向接受新IVDR法规的欧盟及其他地区的实验室。它计划在一年后获得美国食品和药物管理局的许可,在美国推广该平台,Bouwman 补充说:“为了在美国取得成功,我们需要一个适合美国客户的平台。我们在美国市场还没有很大的市场份额。”Bouwman 补充说,虽然该公司在开发新的分子诊断检测方法并希望将测试用于到新平台上,但它打算遵循去年完成的市场研究的指导。该研究指出,“传染病检测市场的最大部分是呼吸系统,胃肠道检测试剂盒排第二,而 STI 试剂盒和移植感染的检测也特别受关注。”在短期内,根据当前的客户需求反馈, Siemens正在完成一项多重测试的开发,以检测和区分甲型流感、乙型流感、SARS-CoV-2 和人类呼吸道合胞病毒,检测将适用于Versant kPCR 分子系统。该公司分子试剂研发小组负责人 Michael Schleichert 表示,预计很快将推出带有 CE-IVD 标志的检测,并专注于向欧洲、中东和非洲地区的医院实验室推销该检测。“随着大流行成为地方病,我们相信 SARS-CoV-2 将成为许多呼吸道病原体实验室想要监测的一种,”Schleichert 在 ECCMID 上说。他指出,总体而言,Siemens已经在营销基于分子检测的呼吸检测,FTD 有可区分 21 种呼吸道病原体的试剂盒。
西门子要做下一代高检测通量分子系统,尽管根据外媒报道还只是找合作伙伴的阶段,却已经定下来3年内上市销售,真可谓是高调宣布入局,这个玩儿法有点不走寻常路,,不知看到这个消息,罗氏等友商将会作何打算。也许本来就是老大罗氏的大通量分子检测系统的炒得轰轰烈烈很有存在感让西门子也不淡定了,也许是新冠疫情催生了分子市场让它也无法避免诱惑,忍不住了终于躬身入局,不管为何,分子这块蛋糕,拿起刀叉、筷子的食客越来越多,谁能突出重围,中国企业又将何时以何种方式占有一席之地乃至领先地位?我们拭目以待。
普瑞纯证服务号现已开通
快来关注【新】鲜上线的普瑞服务号!
↓↓↓点击关注↓↓↓
每周汇总全球法规一线更新!
加入行业粉丝群请加小编:purefda02
业务咨询微信号:purefda
或扫码添加顾问,享受咨询服务
↓ ↓ ↓

普瑞纯证是全球首家SaaS+Data的新型数字化跨境医疗器械CRO企业,我们的全球服务网络分布在包括中国、美国、英国、德国、荷兰、波兰、马耳他、香港等多个国家和地区。
依托法规认证与临床经验丰富的全球顶尖专家服务团队,普瑞纯证为医疗器械、体外诊断、医疗软件AI等产品提供全球市场合规准入的全流程咨询服务,涵盖器械法规咨询,当地授权代表,产品认证注册,海外临床试验,技术文档与体系辅导,产品检测等全流程服务。