热烈祝贺:锦瑞生物快速抗原检测产品进入欧盟通用名单 (HSC RAT Common List)!!

医疗器械 | 出口 | 认证 | FDA CE | 行业热点 | 全球业务

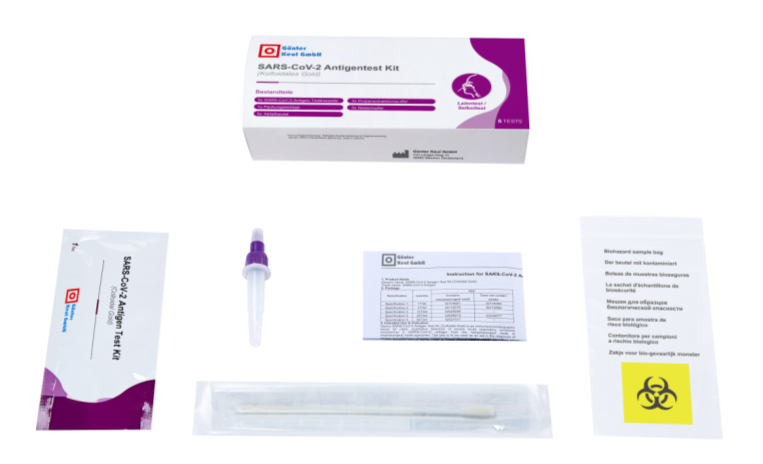
在获得40多个国家的专业使用抗原认证之后,锦瑞生物在普瑞纯证的助力下,其产品新冠病毒抗原检测试剂盒(胶体金法)获准进入欧盟快速抗原检测通用名单。
欧盟卫生安全委员会(HSC)在过去的几个月内,多次提高通用名单申请门槛,致使厂家在申请时也将面临更高挑战。普瑞纯证在协助提交资料的同时,也会对资料内容进行审核并根据最新标准提供修改建议。

01
欧盟快速抗原检测
通用名单最新基本要求
2. 如欧盟验证方无测试报告提供(例如:PEI),则需额外提供第三方独立机构进行临床测试的测试报告与原始数据,此测试与通过PEI验证的采集方式需相同;
3. 提供相应第三方独立机构验证所使用的产品说明书;
4. 此名单只适用于专业版快速抗原检测试剂盒。

02
深圳市锦瑞生物科技有限公司

深圳市锦瑞生物科技有限公司创立于2004年,是一家专业从事临床医疗检验仪器和试剂研发、生产、销售及服务的高科技企业,并且是首批国家级高新技术企业及深圳市软件企业。

其在国内设有28个省级办事机构,在东南亚、中东、非洲、南美洲等地区的部分国家也建立了办事机构,销售及客户服务网络覆盖了全球大多数区域。可为临床医疗检验科室提供满足临床使用需求、高性价比的较为全面的系列化产品和服务。目前全球范围内已有超过100个国家和地区使用锦瑞生物的产品。

专业的事情就要交给专业的人来做,普瑞纯证具有丰富的认证经验,熟悉认证流程,精通认证法规,能高效地为企业提供全方位的支持和解答,针对不同企业,不同产品开发阶段、定制适合的解决方案。
现可为美国,欧洲,加拿大,巴西等多个国家地区提供医疗器械的出口认证、检测、清关物流、渠道对接、数据查询等服务。
有这方面需求的客户欢迎随时联系普瑞君哦!(微信号:purefda)

推荐阅读
关于我们

美国医疗器械注册认证服务 美国食品药品监察局FDA,厂家注册和产品登记认证,510K和NIOSH认证服务 欧盟医疗器械认证服务 欧洲技术文件编写,欧盟CE、MDR、IVDR认证 中国、巴西、加拿大、澳洲、韩国医疗器械认证服务 中国NMPA、巴西ANVISA认证,加拿大MDEL/MDL认证,澳洲ARTG认证,韩国MFDS认证 医疗软件AI注册认证服务 质量管理体系建立,委托检验,临床评价,注册认证申报

